Virus Zika y embarazo
Sección: Revisiones
Autores
1 Eduardo Martínez Martín, 2 Dolores Macarro Ruiz, 3 Paloma Martínez Galán, 4 Javier Manrique Tejedor, 5 Miguel Ángel García Rebollo
1 Matrón Hospital General de Segovia.
2 Matrona Hospital Virgen del Puerto (Plasencia).
3 Matrona Hospital Virgen de la Salud (Toledo).
4 Matrón Hospital Universitario Joan XXIII (Tarragona).
5 Matrón Hospital Materno-Infantil de Badajoz.
Contacto:
Email: edumartinez25@hotmail.com
Titulo:
Virus Zika y embarazo
Resumen
El virus Zika (VZ) pertenece a la familia Flaviviridae, el mismo al que pertenecen el virus del dengue, la fiebre amarilla o la encefalitis japonesa. La enfermedad no está presente en Europa, aunque podría emerger como consecuencia de su rápido avance en el continente americano y de la expansión del vector por el mundo, incluyendo Europa.
La enfermedad por VZ presenta una sintomatología por lo general leve que puede pasar desapercibida o diagnosticarse erróneamente como dengue, chikungunya u otras patologías virales que cursen con fiebre y exantema.
También se ha relacionado con la aparición de alteraciones neurológicas en recién nacidos, como microcefalias, calcificaciones cerebrales y lesiones oculares. Como dato relevante, debemos alertar que una estimación del 80% de las personas infectadas por el VZ es asintomática. En mujeres gestantes la posibilidad de infección por VZ puede ocurrir a cualquier edad gestacional y en teoría con una morbilidad para el feto dependiendo del trimestre en que se produzca la transmisión materno-fetal. El mayor riesgo de microcefalia y malformaciones parece estar asociada con la infección Zika durante el primer trimestre.
La pertinencia de esta revisión radica en que si bien son un grupo susceptible de padecer esta infección, no constituye una población con mayor riesgo de infectarse. Sin embargo, a ellas especialmente deben ir dirigidas las recomendaciones y acciones de promoción y prevención con base en la evidencia disponible que relaciona la infección por VZ con la aparición de anomalías congénitas, siendo el primer trimestre de embarazo el periodo de mayor riesgo de afectación fetal.
Palabras clave:
Title:
Abstract:
Zika virus (ZV) belongs to Flaviviridae family, also including dengue, yellow fever, and Japanese encephalitis viruses. Currently, ZV disease is not present in Europe, although it could emerge due to its quick spreading through the Americas and to the dissemination of its vector all over the world, including Europe.
ZV disease symptoms are usually mild and can even be unnoticed or be mistaken as dengue, chikungunya or other viral diseases causing fever and rash.
It has also been associated to newborn neurological abnormalities, such as microcephalus, brain calcifications and eye lesions. As a relevant finding, it should be stressed that an estimated 80% of people infected with ZV are symptom-free. In pregnant women, ZV infection can occur at any gestational age and, theoretically, fetal morbidity depends on the pregnancy trimester in which mother-to-fetus transmission occurs. Highest risk for microcephalus and malformations appears to be related to Zika infection during the first trimester.
Main relevance of the present review is due to fact that, although this is a group susceptible to infection, pregnant women do not show a higher risk of infection. However, this is the main target group for recommendations and actions to promote prevention based on available evidence indicating an association of ZV infection with congenital abnormalities, with first trimester being the period with a highest risk for fetal involvement.
Keywords:
Zika virus; infection; pregnancy
Introducción
El virus Zika (VZ) pertenece a la familia Flaviviridae, género Flavivirus, el mismo al que pertenecen el virus del dengue, la fiebre amarilla o la encefalitis japonesa. Fue descubierto por primera vez en 1947, en el bosque Zika en Uganda, durante estudios de vigilancia de fiebre amarilla selvática en monos Rhesus1. La presencia del virus en humanos, considerado en un principio huésped ocasional, se constató a través de estudios serológicos en 19522 y no fue hasta 1968 cuando se logró aislar el virus a partir de muestras humanas en Nigeria3.
Hasta 2007 solo se habían descrito casos esporádicos en algunos países de África y Asia. El primer caso autóctono en las Américas fue notificado en febrero de 2014 por el Ministerio de Salud de Chile (Isla de Pascua)4. Pero desde febrero de 2015 se ha verificado un importante incremento de casos por el Ministerio de Salud de Brasil5.
Hasta el 20 de enero de 2016 los países y territorios que han confirmado circulación autóctona de VZ son los siguientes: Brasil, Barbados, Colombia, Ecuador, El Salvador, Guatemala, Guayana, Guyana Francesa, Haití, Honduras, Martinica, México, Panamá, Paraguay, Puerto Rico, San Martin, Guadalupe, Surinam, Venezuela y Bolivia. Fuera de la Región de las Américas, Cabo Verde ha detectado por primera vez casos confirmados de enfermedad por VZ6.
Con base en los distintos hallazgos, la Organización Panamericana de la Salud ha hecho públicas diferentes alertas epidemiológicas (mayo, noviembre y diciembre 2015)1,7,8 y dos actualizaciones epidemiológicas (octubre 2015 y enero 2016)9,10.
La enfermedad no está presente en Europa aunque podría emerger como consecuencia de su rápido avance en el continente americano y de la expansión del vector por el mundo, incluyendo Europa11. Uno de los vectores competentes para la transmisión del VZ, el Ae. albopictus, está presente en una parte importante del territorio español. Desde su primera detección en 2004 el vector se ha establecido en 14 provincias de siete comunidades autónomas: Cataluña, Comunidad Valenciana, Murcia, Baleares, Andalucía, País Vasco y Aragón12,13.
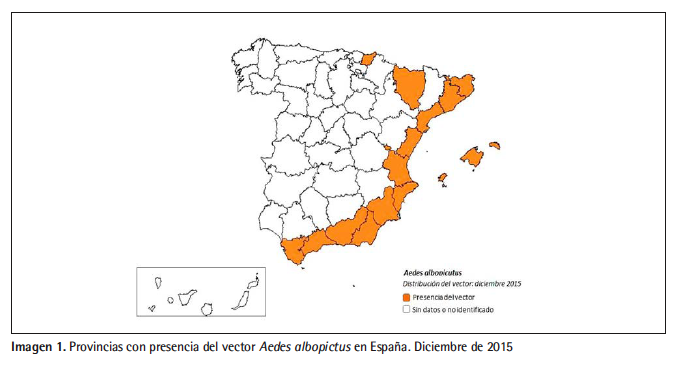 La probabilidad de que exista transmisión del VZ en España va a depender de los siguientes factores:
La probabilidad de que exista transmisión del VZ en España va a depender de los siguientes factores:
- La presencia del vector en el entorno.
- La introducción del virus por un viajero infectado procedente de áreas endémicas.
- La presencia de población susceptible a la infección.
- La coincidencia en el espacio y en el tiempo de un caso importado virémico con el vector.
- La posibilidad de que el virus encuentre las condiciones favorables para su transmisión.
Estos factores están presentes en España en distinta magnitud en las zonas geográficas donde el vector competente está presente, especialmente durante los meses de mayo a octubre. La intensidad de dicha transmisión, en caso de producirse, dependerá de la abundancia del vector en cada lugar y la afluencia de personas infectadas procedentes de zonas endémicas durante los meses que el vector está activo. Dada la alta incidencia de la enfermedad en zonas endémicas con estrecha relación con España y la susceptibilidad a la infección de toda la población española, al no haber estado en contacto previo con este virus, existe un riesgo de transmisión autóctona del VZ real durante el periodo de actividad vectorial en España. El riesgo de transmisión casi desaparece durante el periodo invernal, dada la dudosa actividad vectorial durante este periodo, en todo caso asociada a las condiciones climáticas favorables que en ocasiones tienen lugar en zonas limitadas de la costa mediterránea.
Desde 2013 se han notificado seis casos importados en Europa, procedentes de Tailandia, Polinesia, Brasil y Haití14-16. En España hasta febrero de 2016 se han notificado cinco casos, dos casos de Zika declarados en Cataluña y dos en Castilla y León, corresponden a viajeros que han regresado de países sudamericanos, y un caso en la Comunidad de Madrid en una mujer embarazada.
La enfermedad por VZ presenta una sintomatología por lo general leve que puede pasar desapercibida o diagnosticarse erróneamente como dengue, chikungunya u otras patologías virales que cursen con fiebre y exantema17 (Tabla 1). Los síntomas principales quedan reflejados en la Tabla 2.

El VZ puede producir síndromes neurológicos como el síndrome de Guillain-Barré (SGB), meningoencefalitis, mielitis, entre otros. También se ha relacionado con la aparición de alteraciones neurológicas en recién nacidos (RN). Las autoridades sanitarias de la Polinesia Francesa han notificado recientemente un incremento inusual de malformaciones del sistema nervioso central durante el periodo 2014-2015, coincidiendo con los brotes de VZ en la isla.
Recientemente el Ministerio de Salud de Brasil ha notificado un aumento inusual de la incidencia de microcefalia en RN en varios estados del noreste del país en los que también se ha detectado circulación de VZ. Así como lesiones oculares en la región macular y calcificaciones cerebrales. Aunque aún no fue establecida la relación causal con VZ, no se puede descartar esa hipótesis.
El periodo de incubación oscila entre 3 y 12 días y la duración de la sintomatología entre 2 y 7 días (31). Las infecciones asintomáticas son frecuentes y se estima que tan solo 1 de cada 4 infectados desarrolla clínica18-20.
La transmisión del virus se produce a través de la picadura del mosquito vector. En humanos el virus se ha detectado en sangre, saliva, orina, semen y leche materna19,21,22. Hasta la fecha no se ha documentado ningún caso de infección por VZ por transmisión sanguínea. Sin embargo, un estudio en donantes de sangre asintomáticos durante el brote del 2013-2014 en la Polinesia francesa encontró un 3% de positividad para VZ, por lo que no se puede descartar la posibilidad de transmisión a través de transfusiones sanguíneas19. Respecto a la transmisión sexual, la evidencia existente apoya la posibilidad de transmisión por esta vía. En todo caso, no se conoce el papel que pueden jugar estos posibles modos de transmisión en la extensión de la enfermedad.
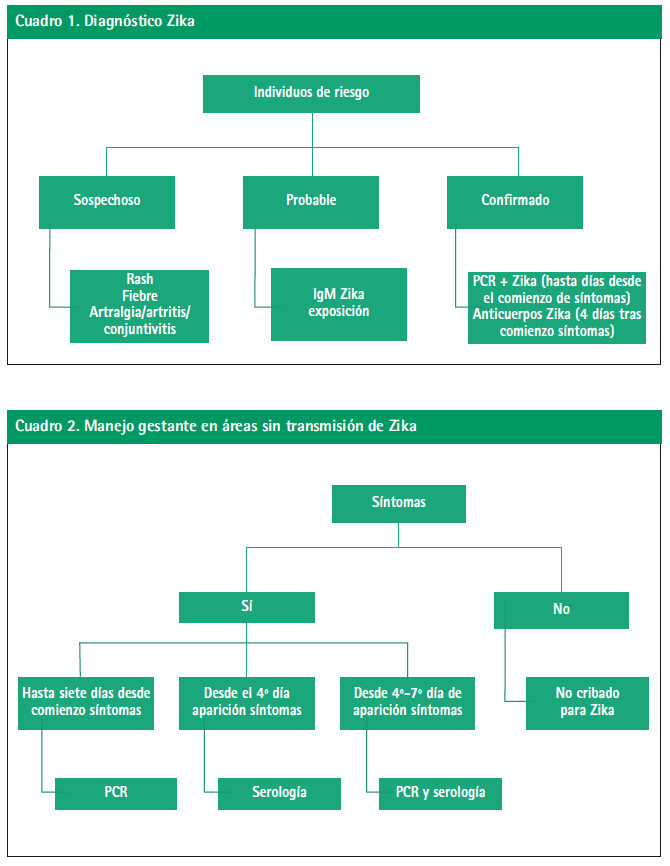
El diagnóstico de confirmación de laboratorio se basa en el aislamiento del virus o en su detección por PCR en muestra clínica23 o a través de pruebas serológicas. El periodo virémico es corto, siendo el virus detectable en sangre aproximadamente entre el tercer y quinto día tras la aparición de síntomas17. La detección de anticuerpos IgM e IgG es posible a través de ELISA e inmunofluorescencia. Los anticuerpos pueden detectarse en suero a partir del quinto o sexto día tras el inicio de la sintomatología aunque los resultados han de interpretarse con cautela pues se han notificado falsos positivos por reacciones cruzadas producidas por otros flavivirus, en este caso sería necesaria un test de neutralización para confirmar la infección23,14. En España, el Centro Nacional Microbiología tiene capacidad para la detección del VZ.
Objetivo
El propósito u objetivo de esta revisión es brindar a los profesionales de salud que asisten a mujeres gestantes, información actualizada con base en las mejores evidencias disponibles para ayudar a prevenir la infección, dar seguimiento a las mujeres embarazadas, así como notificar el caso a las autoridades sanitarias competentes.
Metodología
Se llevó a cabo una revisión narrativa, para lo cual se hizo una búsqueda a través de la consulta de las siguientes bases de datos: PubMed/Medline, Uptodate, Scielo, Cuiden, Cochrane Plus y Google Académico.
Se utilizaron y combinaron los términos “Zika virus”, “infection”, “pregnancy” ”virus Zika”, “infección” y “embarazo”.
Se emplearon los operadores boléanos “OR” y “AND” para combinar los distintos componentes de la búsqueda.
Para refinar la búsqueda se establecieron como límites el idioma (inglés, español y portugués) y la fecha de publicación (los últimos cinco años).
 Se efectuó la identificación de los documentos para su lectura y evaluación aplicando los criterios de inclusión y exclusión (Tabla 3).
Se efectuó la identificación de los documentos para su lectura y evaluación aplicando los criterios de inclusión y exclusión (Tabla 3).
Resultados/discusión
Como dato relevante, se debe alertar que una estimación del 80% de las personas infectadas por el VZ es asintomáticas24,25.
En cuanto a las posibles complicaciones asociadas a la enfermedad por VZ, se ha relacionado con la aparición de alteraciones neurológicas en RN. En 2007 en las islas de Micronesia no se describieron defectos de nacimiento en el momento del brote, tal vez debido al tamaño relativamente pequeño de la población4. Sin embargo, durante el periodo 2014-2015 en la Polinesia francesa fueron notificadas 17 malformaciones neurológicas en RN cuando en los años previos lo notificado estaba entre 0-2, y se hallaron anticuerpos frente a VZ en muestras de cuatro de las madres, lo que sugirió una posible infección durante el embarazo20.
Recientemente Brasil ha notificado un aumento inusual de la incidencia de microcefalia en RN. Desde principios de 2015 hasta la semana epidemiológica 1 de 2016, se registraron 3.530 casos de microcefalia, incluidos 46 fallecidos. Entre 2010 y 2014, en el ámbito nacional, se registraron en promedio anual 163 casos de microcefalia26. Respecto al aumento de los casos de microcefalia y/o malformaciones congénitas aún no hay notificación de otros países donde se han producido brotes de VZ. En estos momentos se están llevando a cabo investigaciones para determinar la relación entre la infección por VZ y la aparición de microcefalia en RN.
Se ha detectado la presencia del VZ en muestras de líquido amniótico de dos mujeres embarazadas con signos fetales de microcefalia. También, se verificó la presencia del genoma del VZ en muestras de tejidos y sangre de un RN fallecido y portador de microcefalia7. Un reciente estudio realizado por Fiocruz-Paraná confirmó la presencia del virus en placenta27.
Además, las autoridades de salud brasileñas han confirmado la detección del genoma de VZ en cuatro casos de malformación congénita. Los casos corresponden a dos abortos y a dos RN a término (37 y 42 semanas de gestación respectivamente) que fallecieron en las primeras 24 horas de vida. Las muestras de tejido de ambos RN resultaron positivas para VZ28,29. En EE.UU., el Departamento de Salud de Hawai ha confirmado el 15 de enero de 2016 la identificación de VZ en un RN con microcefalia cuya madre residió en Brasil en mayo de 201530.
En estos primeros meses de 2016, se ha informado sobre la detección de lesiones oculares en la región macular y calcificaciones cerebrales en tres RN con microcefalia con posible infección intrauterina por VZ. Los tres RN presentaron trastornos de pigmentación en la región macular y pérdida del reflejo foveal unilaterales. En uno de los RN se detectó además atrofia macular neurorretiniana31.
La transmisión materno-fetal del VZ puede ocasionar una infección congénita1,2,6,31.
Hasta la fecha no se ha documentado ningún caso de transmisión de la infección por el VZ a través de la lactancia materna6,23. Sin embargo, la transmisión de algunos otros flavivirus a través de la leche materna se ha descrito32,33.
En mujeres gestantes, la posibilidad de infección por VZ puede ocurrir a cualquier edad gestacional32-34 y en teoría con una morbilidad para el feto dependiendo del trimestre en que se produzca la transmisión materno-fetal, sin embrago, hay que ser concluyentes en el hecho de que la incidencia de infección no está claramente conocida ni suficientemente controlada por este motivo, por lo que los informes y datos sobre las mujeres gestantes infectadas son muy limitados.
El mayor riesgo de microcefalia y malformaciones parece estar asociada con la infección Zika durante el primer trimestre31. La tasa de transmisión vertical y la velocidad a la que los fetos infectados manifiestan complicaciones son desconocidos34. No existe evidencia que sugiera que las gestantes sean una población más susceptible de adquirir la infección del VZ o que se manifieste con más virulencia durante la gestación. La transmisión materno-fetal ha sido y está suficientemente documentada en cada momento evolutivo de la gestación4,7,8, sin embargo el VZ que ha podido ser detectado en muestras o especímenes patológicos de pérdidas fetales o abortos no ha podido demostrar que fuera la causa de dichas pérdidas4.
Los estudios actuales están bajo estrictas líneas de investigación, sobre todo la asociación de VZ y la microcefalia, incluyendo el papel de otros factores que también contribuyen a la aparición de microcefalia como infecciones previas o coincidentes por otros gérmenes distintos al VZ, la malnutrición, hábitos tóxicos, agentes ambientales, antecedentes genéticos, etc.). El total de agentes, el amplio espectro de factores y resultados que pueden asociarse con la infección por VZ durante la gestación, es desconocido y requiere de mucha y extensa investigación para poder poner de manifiesto la evidencia de la relación VZ/microcefalia como única etiología de esta grave malformación fetal.
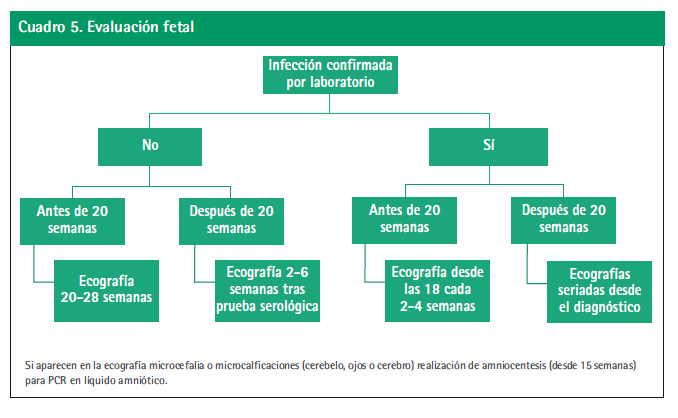
Debido a que no hay tratamiento específico contra esta infección, lo preventivo sigue siendo lo primordial. En tal sentido se debe seguir promoviendo la captación precoz de las mujeres gestantes para realizar las consultas antenatales de acuerdo a las normas nacionales y brindar información sobre las medidas ambientales e individuales para reducir el riesgo de picadura del mosquito transmisor del VZ (Tabla 4). Especial atención se debe dar a los exámenes rutinarios para sífilis, toxoplasmosis, citomegalovirus y rubéola, que serán relevantes en caso de necesitar confirmación etiológica ante un defecto congénito.
 Hasta el momento, ha sido una enfermedad relativamente leve, con alcance limitado, pero su verdadero potencial como un virus y como agente de la enfermedad se desconoce actualmente. Todavía no se ha informado sobre ninguna muerte atribuida a la infección por VZ en ninguno de los brotes registrados.
Hasta el momento, ha sido una enfermedad relativamente leve, con alcance limitado, pero su verdadero potencial como un virus y como agente de la enfermedad se desconoce actualmente. Todavía no se ha informado sobre ninguna muerte atribuida a la infección por VZ en ninguno de los brotes registrados.
Conclusiones
Existe un riesgo de introducción y transmisión autóctona del VZ en España, considerando la rápida expansión del virus por las regiones de América y la frecuente comunicación de España con estos países, por lo que es recomendable establecer una vigilancia específica de la enfermedad del VZ y difundir entre los profesionales sanitarios para que los casos importados se detecten lo antes posible para prevenir transmisiones autóctonas.
Las mujeres gestantes son un grupo susceptibles de padecerla, pero no constituye una población de más riesgo de infección. Sin embargo, a ellas especialmente deben ir dirigidas las recomendaciones y acciones de promoción y prevención con base en la evidencia disponible, que relaciona la infección por VZ con la aparición de anomalías congénitas, siendo el primer trimestre de embarazo el periodo de mayor riesgo de afectación fetal.
Es importante reforzar, a través de los servicios de Sanidad Exterior y de atención al viajero, las recomendaciones para viajeros internacionales. A pesar del aparente riesgo latente dado que el binomio ambiente/población de Aedes Aegypti es prácticamente desfavorable para estos últimos, hasta el punto de ser una anécdota por el momento su presencia en los ámbitos europeos, debemos estar alerta y evitar la expansión de aquellos mosquitos detectados en el área mediterránea y en otra zonas de Europa.
Anexo
Bibliografía
- Organización Panamericana de la Salud. Alerta Epidemiológica Infección por virus Zika. [acceso 10 marzo 2016]. Disponible en: http://www.paho.org/hq/index.php?option=com_docman&task=doc_view&Itemid=&gid=30076&lang=es
- Dick GWA, Kitchen SF, Haddow AJ. Zika virus. II. Pathogenicity and physical properties. Trans R Soc Trop Med Hyg. 1952; 46(5):521-34.
- Fagbami AH. Zika virus infections in Nigeria: virological and seroepidemiological investigations in Oyo State. J Hyg (Lond). 1979; 83(2):213-9.
- Ministerio de Salud de Chile. Instituto de Salud Pública confirma el primer caso en el país de infección por virus Zika (ZIKAV) [acceso 10 marzo 2016]. Disponible en: http://www.ispch.cl/noticia/20750
- Ministério da Saúde (Brasil). Confirmação do Zika Vírus no Brasil, [Internet]. Brasília. Ministério da Saúde (Brazil); 2015 [acceso 10 marzo 2016]. Disponible en: from: http://portalsaude.saude.gov.br/index.php/cidadao/principal/agencia saude/17701-confirmacao-dozika-virus-no-brasil
- Ministério da Saúde. Capo verde. Ministério da Saúde confirma infecção por Vírus Zika no concelho da Praia [Internet]. 2015 [acceso 10 marzo 2016]. Disponible en: http://www.minsaude.gov.cv/index.php/rss-noticias/912-ministerio-da-saude-confirma-infeccao por-virus-zika-no-concelho-da-praia
- Organización Panamericana de la Salud. Alerta Epidemiológica síndrome neurológico, anomalías congénitas e infección por virus Zika. Implicaciones para la salud pública en las Américas [acceso 10 marzo 2016]. Disponible en: http://www.paho.org/hq/index.php?option=com_docman&task=doc_view&Itemid=270&gid=32404&lang=es
- Organización Panamericana de la Salud. Alerta Epidemiológica Incremento de microcefalia en el nordeste de Brasil [acceso 10 marzo 2016]. Disponible en: http://www.paho.org/hq/index.php?option=com_docman&task=doc_view&Itemid=270&gid=32286&lang=es
- Organización Panamericana de la Salud. Actualización Epidemiológica. Infección por virus Zika [acceso 10 marzo 2016]. Disponible en: http://www.paho.org/hq/index.php?option=com_docman&task=doc_view&Itemid=270&gid=32023&lang=es
- Organización Panamericana de la Salud. Actualización Epidemiológica. Síndrome neurológico, anomalías congénitas e infección por virus Zika. [acceso 10 marzo 2016]. Disponible en: http://www.paho.org/hq/index.php?option=com_docman&task=doc_view&Itemid=270&gid=32876&lang=es
- Kirya BG, Okia NO. A yellow fever epizootic in Zika Forest, Uganda, during 1972: Part 2: Monkey serology. Trans R Soc Trop Med Hyg. 1977; 71(4):300-3.
- Alarcón Elbal P. Primeros hallazgos de Aedes (Stegomyia) albopictus (Skuse, 1894) en la provincia de Valencia, España. Anales de Biología. 2013; 35:95-9.
- Torrell Sorio, A, Fernández Rodríguez J. Caracterització de la població del mosquit tigre asiàtic (Aedes albopictus) a Catalunya 2008. Direcció General del Medi Natural/Generalitat de Catalunya; 2008.
- Tappe D, Rissland J, Gabriel M, Emmerich P, Gunther S, Held G, et al. First case of laboratory-confirmed Zika virus infection imported into Europe, November 2013. Euro Surveill. 2014; 19(4).
- Zammarchi L, Stella G, Mantella A, Bartolozzi D, Tappe D, Gunther S, et al. Zika virus infections imported to Italy: clinical, immunological and virological findings, and public health implications. J Clin Virol. 2015; 63:32-5.
- Zammarchi L, Tappe D, Fortuna C, Remoli ME, Gunther S, Venturi G, et al. Zika virus infection in a traveller returning to Europe from Brazil, March 2015. Euro Surveill. 2015; 20(23).
- Loos S, Mallet H-P, Leparc Goffart I, Gauthier V, Cardoso T, Herida M. Current Zika virus epidemiology and recent epidemics. Med Mal Infect. 2014; 44(7):302-7.
- Duffy MR, Chen T-H, Hancock WT, Powers AM, Kool JL, Lanciotti RS, et al. Zika virus outbreak on Yap Island, Federated States of Micronesia. N Engl J Med. 2009; 360(24):2536-43.
- Musso D, Nhan T, Robin E, Roche C, Bierlaire D, Zisou K, et al. Potential for Zikavirus French Polynesia, November 2013 to February 2014. Euro Surveill. 2014; 19(14):11.
- Organización Panamericana de la Salud. Alerta Epidemiológica. Síndrome neurológico, anomalías congénitas e infección por virus Zika. Implicaciones para la salud pública en las Américas. [Internet]. 2015 [acceso 10 marzo 2016]. Disponible en: Recuperado a partir de:file:///D:/usuarios/sgilt/Downloads/2015-dic-1-cha-alerta-epi-zika-sindromeneuro.pdf
- Musso D, Roche C, Nhan T-X, Robin E, Teissier A, Cao-Lormeau V-M. Detection of Zika virus in saliva. J Clin Virol. 2015; 68:53-5.
- Besnard M, Lastere S, Teissier A, Cao-Lormeau V, Musso D. Evidence of perinatal transmission of Zika virus, French Polynesia. Euro Surveill 2014; 19(13).
- Balm MND, Lee CK, Lee HK, Chiu L, Koay ESC, Tang JW. A diagnostic polymerase chainreaction assay for Zika virus. J Med Virol. 2012; 84(9):1501-5.
- Lanciotti RS, Kosoy OL, Laven JJ, Velez JO, Lambert AJ, Johnson AJ, et al. Genetic and serologic properties of Zika virus associated with an epidemic, Yap State, Micronesia, 2007. Emerg Infect Dis. 2008; 14(8):1232-9.
- Duffy MR, Chen TH, Hancock WT. Zika virus outbreak on Yap Island, Federated States of Micronesia. N Engl J Med 2009; 360:2536-43.
- Centro de operaciones de emergências em saúde pública sobre microcefalias. Monitoramento dos casos de microcefalias no Brasil. Informe epidemiológico Núm. 08 Semana epidemiológica 1/2006.
- ASCOM Fiocruz-Paraná. Pesquisa da Fiocruz Paraná confirma transmissão intra-uterina do zika virus. [Internet]. Paraná; 2016 [acceso 10 marzo 2016]. Disponible en: http://www.icc.fiocruz.br/pesquisa-da-fiocruz-parana-confirma-transmissao-intra-uterina-do-zika-virus/
- Organización Panamericana de la Salud. Actualización Epidemiológica. Síndrome neurológico, anomalías congénitas e infección por virus Zika. 2016. [Internet]. [acceso 10 marzo 2016]. Disponible en: http://www.paho.org/hq/index.php?option=com_topics&view=article&id=427&Itemid=41484
- European Center for Disease Prevention and Control. Rapid Risk Assessment. Microcephaly in Brazil potentially linked to the Zika virus epidemic-24 Nov 2015. Stockholm: ECDC; 2015.
- Confirmation of Zika infection inbaby born with microcephaly. [Internet]. Hawaii Department of Health. News Release Jan. 15, 2016. [acceso 10 marzo 2016]. Disponible en: http://khon2.com/2016/01/15/hawaii-baby-with-birth-defect-was-infected-with-zika-virus/
- Ventura CV, Maia M, Bravo-Filho V, Góis AL, Belfort R Jr. Zika virus in Brazil and macular atrophy in a child with microcephaly. The Lancet. 387(10015):228.
- CDC. CDC health advisory: recognizing, managing, and reporting Zika virus infections in travelers returning from Central America, South America, the Caribbean and Mexico. Atlanta, GA: US Department of Health and Human Services, CDC; 2016. [acceso 10 marzo 2016]. Disponible en: http://emergency.cdc.gov/han/han00385.asp
- Besnard M, Lastere S, Teissier A, Cao-Lormeau V, Musso D. Evidence of perinatal transmission of Zika virus, French Polynesia, December 2013 and February 2014. Euro Surveill 2014; 19:13-6.
- Oliveira Melo AS, Malinger G, Ximenes R, Szejnfeld PO, Alves Sampaio S, Bispo de Filippis AM. Zika virus intrauterine infection causes fetal brain abnormality and microcephaly: tip of the iceberg? Ultrasound Obstet Gynecol 2016; 47:6-7.

